Weet je nog die leskunde over energie die niet verloren gaat, maar alleen van vorm verandert? Misschien voelt het alsof de basisregels van de natuurkunde, die we al een eeuw volgen, plotseling op losse schroeven komen te staan. Een recente doorbraak dwingt wetenschappers om de Eerste Wet van de Thermodynamica écht opnieuw te interpreteren. Dit is cruciaal, want als je dit nu niet begrijpt, loop je de nieuwste inzichten in complexe energiesystemen mis.
De mythe van de perfecte balans
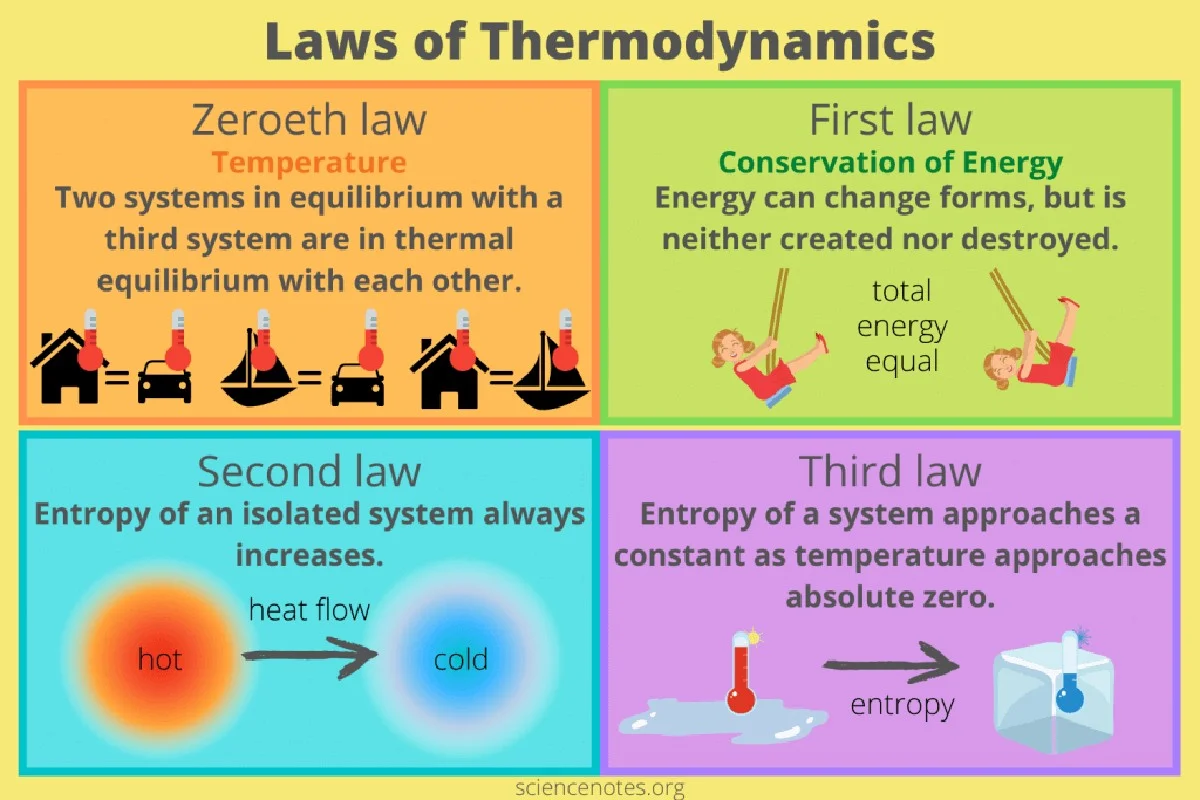
De Eerste Wet van de Thermodynamica klinkt simpel: energie kan niet worden gecreëerd of vernietigd, alleen omgezet. Dat is de les die we op de middelbare school leerden, vaak geïllustreerd met een ballon die opwarmt en uitzet. De totale energie die je erin stopt, leidt tot uitzetting én temperatuurstijging van het gas.
Dit klopte perfect voor systemen die in thermodynamisch evenwicht verkeerden. Denk aan een perfect gemengd kopje thee: overal dezelfde temperatuur. Maar in de echte wereld, en zeker in het heelal, is die gelijkmatigheid zeldzaam.
In de praktijk zien we dit probleem vaak over het hoofd, zelfs met de apparaten die we dagelijks gebruiken – al is het verschil subtiel. We zijn gewend om systemen te analyseren die stabiel zijn, maar systemen buiten evenwicht gedragen zich anders.
Het probleem met 'uit balans' systemen
Wanneer een systeem niet in evenwicht is – stel je voor, er is een hete plek en een koude plek naast elkaar – dan schieten de standaardformules tekort. De klassieke wetten beschreven de energieomzetting bijna volledig met alleen dichtheid en druk.
Onderzoeker Paul Cassak merkte op in een interview voor Popular Mechanics dat de oorspronkelijke wet zich enkel focust op processen die dichtheid en temperatuur veranderen. "Wat wij ontdekten," legt hij uit, "is dat alle andere grootheden die plasma, vloeistof of gas beschrijven als het niet in evenwicht is, buiten de Eerste Wet vallen."
De oplossing die de deur opent naar de kosmos
Wetenschappers zochten al lang naar een manier om die 'missende' energieomzettingen te kwantificeren. Dit is essentieel voor het begrijpen van materie zoals interstellair plasma – denk aan de staarten van kometen of de buitenlagen van sterren.
De doorbraak lag in complexe wiskunde die die extra eigenschappen van de materie buiten evenwicht meeneemt in de energieberekening. Voor een leek lijken dit misschien onbegrijpelijke vergelijkingen, maar voor de natuurkundige is dit het gereedschap dat eeuwenoud denken oprekt.
Wat betekent dit concreet voor jou, zelfs als je geen sterrenkundige bent? Denk aan:
- Verbeterde modellen voor weersvoorspellingen (die ook complexe, niet-evenwicht systemen zijn).
- Nieuwe inzichten in hoe materialen reageren in chemische processen.
- Potentiële stappen richting efficiëntere kwantumcomputers.
Dit soort aanpassingen aan de fundamentele natuurwetten gebeurt niet elk jaar. Het bewijst dat zelfs wetten die al sinds de jaren 1850 bestaan, nog steeds relevant gemaakt kunnen worden als we ze met een frisse blik bekijken en de nuance opzoeken.
Wat is volgens jou het meest verrassende natuurkundige feit dat je ooit op school leerde, maar dat in de praktijk totaal anders bleek te werken?